D-アミノ酸の分析方法 その2
微生物から植物、ヒトを含む哺乳類まで、様々な組織に存在し、生理機能を有することも明らかとなってきたD-アミノ酸。これらの研究が発展してきた基盤には、D-アミノ酸を検出・分析する技術の進歩があります。
生体内のD-アミノ酸はL-アミノ酸などと比べて非常に微量であり,またL-アミノ酸やペプチドなど多種多様な夾雑物の妨害を受けるため,その分析には高い感度と高い選択性、高い分離能が必要となります。分析の感度と選択性、分離能を高めるため、数多くの研究が進められてきました。
今回は遊離型のD-アミノ酸を主に高速液体クロマトグラフィー(HPLC)を用いて分析する方法についてご紹介いたします。
| 分析方法 | ||
|---|---|---|
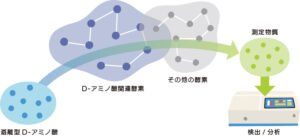
| 遊離型のD-アミノ酸 | 酵素法 | D-アミノ酸酸化酵素を用いたD-アミノ酸全量測定 |
| D-アスパラギン酸オキシダーゼを用いたD-Asp測定 | ||
| アラニン脱水素酵素とアラニンラセマーゼを用いたD-Ala測定 | ||
| D-セリンデヒドラターゼを用いたD-Ser測定 | ||
| HPLC法 | プレカラム誘導体化法(ジアステレオマー法) | |
| キラルカラム法(光学分割カラム法) | ||
| LC/MS/MS法 | ||
| 二次元HPLC法 | ||
| その他 |
ガスクロマトグラフィー (GC)、 高速キャピラリー電気泳動 (HPCE) など |
|
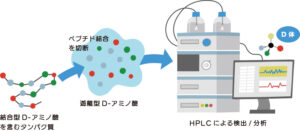
| 結合型のD-アミノ酸 | 加水分解+HPLC分析 | |
| 酵素分解+HPLC分析 | ||
| その他 | 多次元赤外円二色性分光法 など | |
光学(鏡像)異性体であるL体、D体のアミノ酸は構成する原子(団)は同じですが立体的に異なっていて、構造が鏡写しの関係にある物質です。このようなキラル分子の鏡像異性体は物理的性質、化学的性質の多くが同じであり、分離分析するためにはわずかにある性質の違いを利用する必要があります。
前回のコラムでお伝えした、酵素法によるD-アミノ酸の測定では、酵素が立体構造の差異を認識することでD-体のアミノ酸を選択することができました。HPLC法では、別のキラルな化合物に対する反応性がL-アミノ酸とD-アミノ酸とでは異なる性質を利用して、L体とD体を分離(光学分割)、分析します。
① プレカラム誘導体化法(ジアステレオマー法)
遊離D-アミノ酸をHPLCで分析する方法として古くから用いられており、現在でもD-アミノ酸研究の場で広く用いられている方法です。
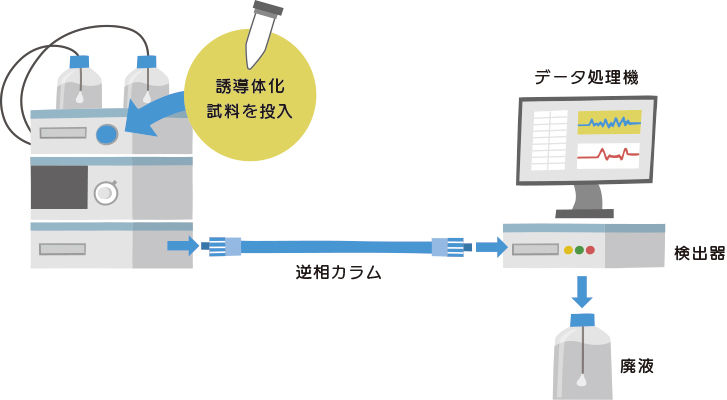
この方法では、HPLCカラムに試料をアプライする前にキラルな試薬と試料中のアミノ酸を反応させてアミノ酸を誘導体化し、生成した化学的性質の異なる立体異性体(ジアステレオマー)を逆相カラムにかけてL体とD体を分離します。性質が非常に似ており分離が困難な鏡像異性体を、キラル試薬と反応させて化学的性質の異なるジアステレオマーに変換することで、光学分割できるようになります。
この方法は汎用性の高い逆相カラムを使用しており、誘導体化に用いるキラル試薬もメーカー各社から市販されています。キラル化合物N-isobutyryl-L-cysteineと蛍光試薬o-phthaldialdehydeを用いて蛍光誘導体化される実施例が見られます。
逆相HPLCのみでは分離能が低いため、微量なD-アミノ酸を検出することが難しい場合やアミノ酸種によっては検出自体が困難な場合がありますが、測定したいD-アミノ酸の種類があらかじめ決まっていて、HPLC装置をお持ちの研究室では比較的廉価簡便に、試料に含まれるD-アミノ酸量を定量分析することができます。
②キラルカラム法(光学分割カラム法)
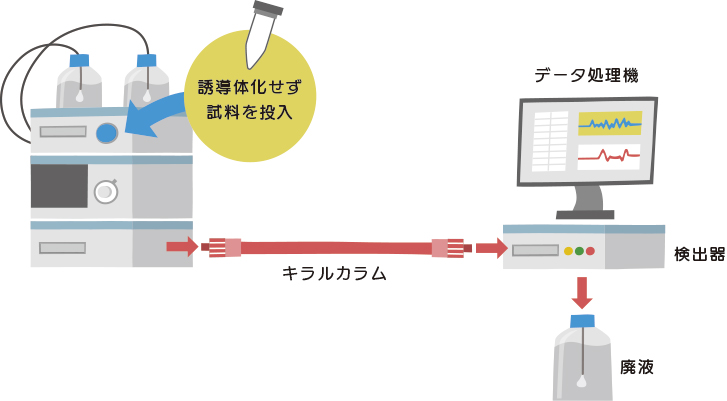
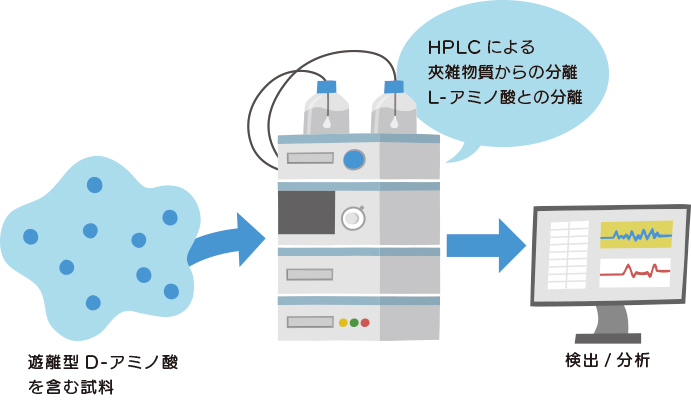
キラルカラム法は、キラルな化合物をHPLCカラムの固定相に利用し、L体とD体を分離する方法です。アミノ酸はカラムの固定相に含まれるキラル化合物との間で可逆的相互作用を形成しますが、その複合体の安定性はL体とD体では異なり、その結果、固定相に対する分配係数に差が生じて光学的に分離でき、L体とD体は異なるピークとして検出することが可能となります。
キラルカラムでは試料に含まれるアミノ酸を誘導体化させる前処理が不要で光学分割は達成されますが、アミノ酸を種別に分離することは困難です。分析試料中の他の夾雑成分からの分離能という点にも課題があり、試料中に1種類のアミノ酸しか存在しないような場合(例えば酵素反応液中の生成D-アミノ酸)であれば有効な手段となりますが、複数のアミノ酸が存在する試料には不適である可能性があります。
D-アミノ酸の生理学的機能が明らかになるにつれて、より微量なD-アミノ酸量を、より高い精度で、より迅速に、アミノ酸種を問わず一斉に、測定する必要性が高まってきました。誘導体化に用いる試薬の開発がすすめられると共に、複数の分析技術を組み合わせることで、迅速で高精度のD-アミノ酸分析を実現できるようになってきました。研究開発された技術の代表例として、実際に商業化されD-アミノ酸分析の受託サービスが行われている2つの方法を取り上げて次にご紹介いたします。
③LC-MS/MS法
HPLCとタンデム四重極型質量分析計(MS/MS)を組み合わせた方法です。
キラル試薬でアミノ酸を誘導体化した後、逆相HPLCでジアステレオマーを分離して、MS/MSで検出・定量します。
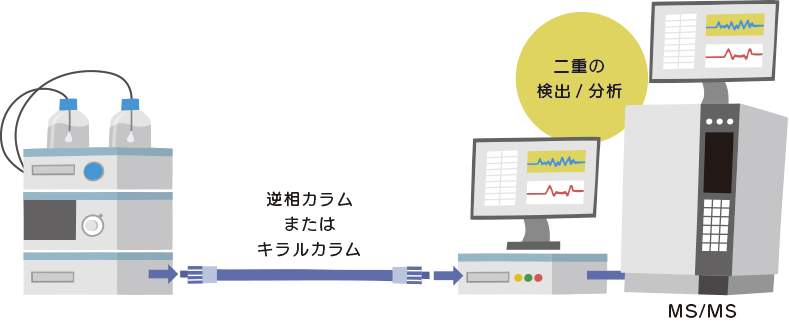
簡便な逆相LCによるキラル分離と質量分析によるアミノ酸の同定を組み合わせた、迅速な一斉分析法として有用で、食品から微生物培養液、血漿、尿などの生体試料まで幅広い検体を対象としています。
誘導体化逆相カラムの代わりに、アミノ酸を誘導体化せずキラルカラムを用いる方法も実施されています。
④二次元HPLC法
プレカラム誘導体化法の逆相カラムとキラルカラム、2本のカラムを繋ぎ合わせて一つの流路として検出、測定します。
この方法では、まず蛍光誘導体化試薬でアミノ酸を誘導体化し,一次元目に逆相カラムで検体内の各アミノ酸を種毎に分離し、それぞれのアミノ酸をD体とL体の混合物として溶出します。各アミノ酸のピークを、バルブを切り替えて分取し、二次元目の光学分割キラルカラムへ導入してD体L体の分離と定量を行います。
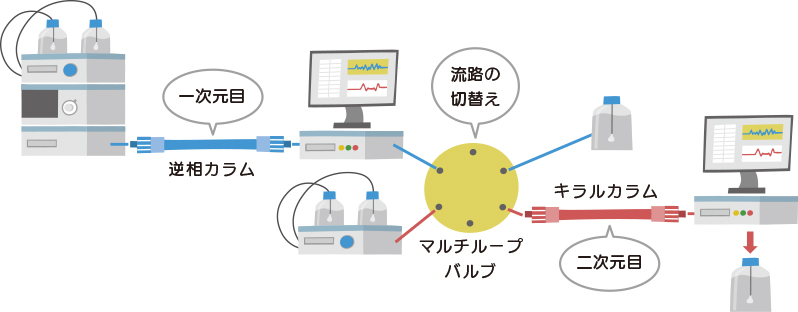
この方法は、強い蛍光を有するアミノ酸誘導体化試薬や独自に設計/作成された専用カラムを用いた多検体の高速ルーティン分析を特長とし、検体内の微量D-アミノ酸を迅速かつ高感度に分析することが可能です。尿などの体液や培地、食品に加えて、腎臓や脳など固形組織中の遊離アミノ酸も分析対象としており、非常に優れたD-アミノ酸一斉分析方法として多方面で応用されています。
今回はD-アミノ酸の分析方法のうち、遊離型のD-アミノ酸を主にHPLCで分析する手法についてご紹介いたしました。ご紹介いたしました上記例のほかにも、複数の分析技術を組み合わせた高精度のD-アミノ酸分析研究は数多く行われています。
次回はタンパク質やペプチド内に含まれた形で存在している、結合型(組織型)のD-アミノ酸分析方法について、いくつかご紹介いたします。
参考・引用文献
- ①プレカラム誘導体化法(ジアステレオマー法)
Atsushi Hashimoto, Toru Nishikawa, Takae Oka, Kiyohisa Takahashi, Tokishi Hayashi: Journal of Chromatography, 582, 41-48 (1992).
Agilent 1290 Infinity Ⅱ LC システムを用いた全自動プレカラム誘導体法によるアミノ酸のキラル分離分析:アジレント・テクノロジー株式会社 - ②キラルカラム法(光学分割カラム法)
板橋豊:化学と生物, 33, 381-388 (1995).
大西敦:オレオサイエンス, 16, 381-386 (2016). - ③LC/MS/MS法
Masashi Harada, Sachise Karakawa, Naoyuki Yamada, Hiroshi Miyano, Kazutaka Shimbo: Journal of Chromatography A, 1593, 91-101 (2019).
Yutaka Konya, Takeshi Bamba, Eiichiro Fukusaki: Journal of Bioscience and Bioengineering, 121, 349-353 (2016).
Yosuke Nakano, Yutaka Konya, Moyu Taniguchi, Eiichiro Fukusaki: Journal of Bioscience and Bioengineering, 123, 134-138 (2017).
D,L-アミノ酸の定性 / 定量分析(LC-MS/MSを用いた分析):株式会社島津テクノリサーチ
(https://www.shimadzu-techno.co.jp/annai/pha/h17.html)
LC/MS/MSによるD、L-アミノ酸の光学分割による定量:株式会社東レリサーチセンター
(http://cs2.toray.co.jp/news/trc/news_rd01.nsf/0/41E60C46C6435FE2492582D600293A06) - ④二次元HPLC法
K. Imai, Y. Watanabe: Analytica Chimica Acta, 130, 377-383 (1981).
今井一洋:薬学雑誌, 123, 901-917 (2003).
浜瀬健司,財津潔:分析化学, 53, 677-690 (2004).
Hamase, K., Morikawa, A., Ohgusu, T., Lindner, W., & Zaitsu, K.: J. Chromatogr. A, 1143, 105‒111 (2007).
Hamase K, Morikawa A, Etoh S, Tojo Y, Miyoshi Y, Zaitsu K.: analytical sciences, 25, 961-968 (2009).
キラルアミノ酸分析受託サービス:株式会社セツロテック (https://www.setsurotech.com/chiral-amino-acid/)