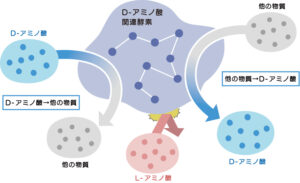
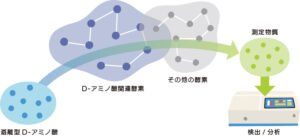
D-アミノ酸の合成方法
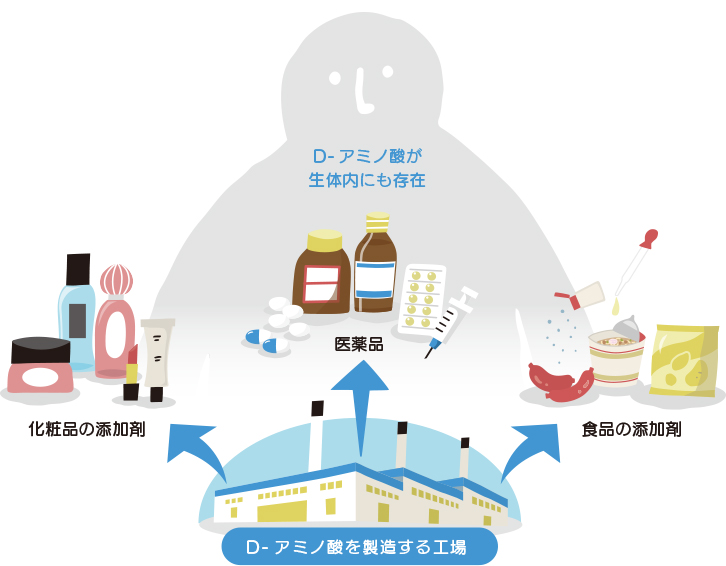
生体中のたんぱく質を構成するアミノ酸はL-アミノ酸であり、光学異性体であるD-アミノ酸は、長年、微生物の細胞壁ペプチドグリカン以外には存在しないと考えられてきました。
しかし、研究が進み、D-アミノ酸が哺乳類を含む高等動物の生体内にも存在し、重要な生理機能を有することが明らかとなってきました。それに伴って現在では、医薬品、農薬や工業製品を製造する中間体として、および食品、化粧品などの添加剤として、D-アミノ酸が用いられるようになっています。
D-アミノ酸の製造方法はいくつかあり、化学的光学分割手法と生物学的手法とに大別されます。
| D-アミノ酸の製造方法 | ||
|---|---|---|
|
化学的手法 |
優先析出法 | ラセミ体のアミノ酸溶液中に一方の活性体の種を加えることによって優先的に一方の結晶のみを成長させる方法 |
| ジアステレオマー法 | ラセミ体のアミノ酸に光学分割剤を作用させて、2種類のジアステレオマーへと誘導し、ジアステレオマー間の溶解度差等を利用してジアステレオマーを分離する方法 | |
| 生物学的手法 | 発酵法 | 微生物に栄養を与えて培養し、微生物が生命活動を行う中でアミノ酸をつくらせる方法 |
| 酵素法 | 微生物に栄養を与えて培養し、微生物が生命活動を行う中でアミノ酸をつくらせる方法 | |
化学的手法としてはラセミ体のアミノ酸を優先晶出法により光学分割する方法や、同じくラセミ体のアミノ酸と他の光学活性化合物との塩を形成してジアステレオマーとして分割する方法などが良く用いられています。
生物学的手法には発酵法と酵素法がありますが、微生物を培養してアミノ酸をつくらせる発酵法ではD-Ala以外のD-アミノ酸を生産できないため、生物学的合成法の主流は、基質となる原料に酵素を反応させてD-アミノ酸を生成する「酵素法」が主流となっています。
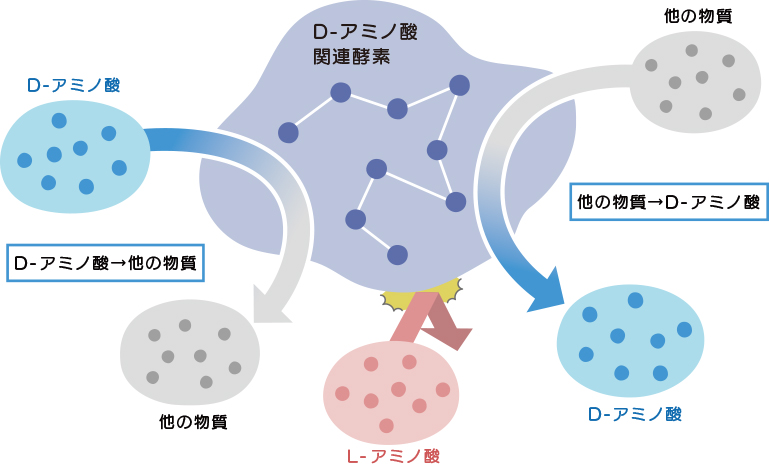
今回は様々なD-アミノ酸製造方法のうち、酵素法についてご紹介いたします。
① N-アシルアミノ酸を基質とした方法
L体とD体両方を含むラセミ体のN-アシルアミノ酸を原料とし、D体に特異的に作用する加水分解酵素(D-アミノアシラーゼ)で分解して、D-アミノ酸を回収する方法です。
必要なD-アミノ酸のみを特異的に生成させる方法であり、1段階反応で光学純度に優れたD-アミノ酸を容易に得ることができます。
この方法においては、D-アミノアシラーゼが基質としないL体である、N-アシル-L-アミノ酸は反応系中に残ったままとなってしまいます。D-アミノ酸の収率を向上させるためには残存したN-アシル-L-アミノ酸をラセミ化してN-アシル-DL-アミノ酸に戻し、再度原料として用いるという工程が必要となります。ここで用いられるのはN-アシルアミノ酸のラセミ化を触媒するN-アシルアミノ酸ラセマーゼという酵素です。この酵素は、N-アシル修飾されていないアミノ酸には作用せず、N-アシルアミノ酸を特異的にラセミ化する酵素であることから、この反応系に用いる有効なラセマーゼとされています。
この2つの酵素を組み合わせることで、原料であるN-アシル-DL-アミノ酸を有効利用することができ、D-アミノ酸を高収率に製造することが可能です。
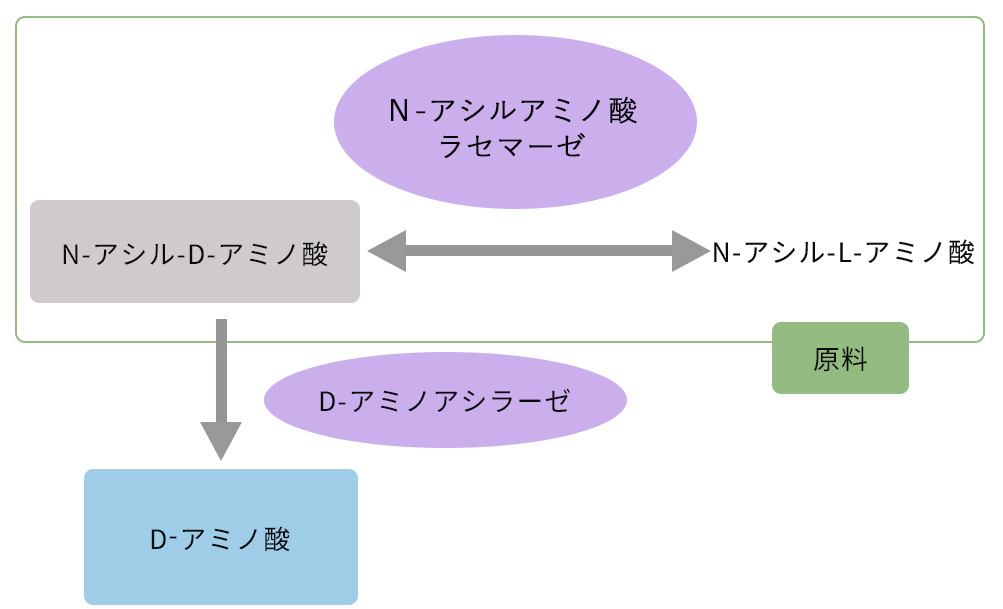
この製造方法においては、基質となるN-アシル-D-アミノ酸に対して、D-アミノアシラーゼとN-アシルアミノ酸ラセマーゼ、2つの酵素が作用することになります。工業的な規模でD-アミノ酸を高収率に得るためには、2つの酵素両方が基質であるN-アシル-D-アミノ酸に対して高い酵素活性を示す必要があります。そのため、基質側のアミノ酸のN-アシル化を改良したり、酵素の組み合わせを変更したり、基質特異性や酵素活性がより高い酵素を探求したりといった研究開発が多く行われました。
② DL-5-置換ヒダントインを基質とした方法
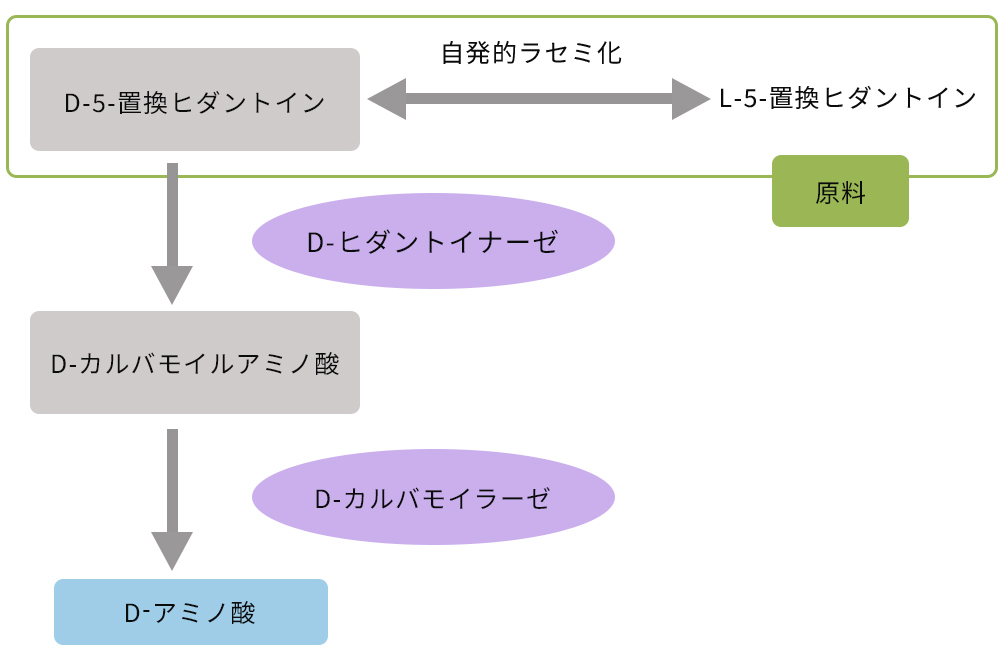
L体とD体両方を含むラセミ体のDL-5-置換ヒダントインを初発の原料(基質)とし、まずD体に特異的に作用するD-ヒダントイン加水分解酵素(D-ヒダントイナーゼ)をDL-5-置換ヒダントイン作用させてD体のみをN-カルバモイル-D-アミノ酸に変換します。次に生成したN-カルバモイル-D-アミノ酸にD-カルバモイラーゼを作用させて脱カルバモイル反応を経て、D-アミノ酸が生成します。
D-ヒダントイナーゼの基質とならず反応液中に残ったL体の5-置換ヒダントインは、先の①N-アシルアミノ酸を基質とした系と同様、ラセマーゼ酵素を用いてラセミ化して再度原料として用いる方法が示されています。他方で、5-置換ヒダントインは微量のアルカリの存在下で極めてラセミ化を受けやすい性質を持つことを利用して、D-ヒダントイナーゼ反応系で自発的にラセミ化してD体に変換させる方法も確立されています。後者の場合、反応液中に残ったL体をD体に変換するための酵素反応工程が不要となりますので、製造プロセスが簡潔になります。
D-カルバモイラーゼが行う脱カルバモイル反応は、亜硝酸酸化などの化学的な脱カルバモイル化を用いている手法も報告されていますが、その際には生成物であるD-アミノ酸がラセミ化しない条件を設定することが重要となっています。
本法の原料となるDL-5-置換ヒダントインは、技術的に確立された方法であるBucherer法により、アルデヒドなどから容易に合成することができます。また、本反応系に用いられている酵素の基質特異性は広く、同一プロセスで広範囲のD-アミノ酸の生産に適用できるとされています。
酵素法には他にも、ラセミ体のDL-アミノ酸にL体のアミノ酸を選択的に分解する酵素を作用させて残存するD-アミノ酸を回収する方法や、α-ケト酸に数種の酵素を作用させてD-アミノ酸を合成する方法、ホルムアルデヒドとグリシンに酵素を反応させてD-Serを合成する方法などが知られています。
D-アミノ酸関連酵素の研究が進んだことや、有機合成の進歩に伴って使用する基質が安価に製造できるようになったことなどがあって、現在までにいくつかの方法が工業化されています。
今回は、各種製造業の原料として用いられているD-アミノ酸の製造方法について、酵素法を中心にご紹介いたしました。
次回は、D-アミノ酸製造やD-アミノ酸研究の発展の基礎となる、D-アミノ酸の分析方法についてお伝えいたします。
参考・引用文献
- 佐藤治代:有機合成化学協会誌,57,323-333 (1999).
- 秋田 紘長,大島 敏久,櫻庭 春彦:生化学,87,582‒590 (2015).
- 特開2008-255010 岩手大学 DL-バリンラセミ化合物の光学分割方法
- 特開2013-241339 三菱瓦斯化学株式会社 光学活性アミノ酸の製造方法
- 特開2004-215656 株式会社ダイセル D-アミノアシラーゼの変異体
- 特開2009-082026 旭化学工業株式会社 D-アミノアシラーゼによるD-アミノ酸の製造方法
- 特開2001-046088 デグサ-ヒュルス アクチェンゲゼルシャフト N-アセチルアミノ酸ラセマーゼ、そのコーディング遺伝子、該遺伝子を有するプラスミド、ベクター及び微生物、該遺伝子のためのプライマー及びゾンデ及び該ラセマーゼの使用
- WO12/002450 積水メディカル株式会社 東洋紡株式会社 D-サクシニラーゼ、およびこれを用いたD-アミノ酸の製造方法
- 横関健三:醸造協会誌,83,230-237 (1988).
- 高橋里美:発酵工学会誌,61,139-151 (1983).
- 特開2005-278468 味の素株式会社 光学活性アミノ酸の製造方法
- 特開2007-189949 株式会社カネカ 新規ヒダントイナーゼ及び光学活性アミノ酸誘導体の製造方法
- 高橋里美, 難波弘憲, 池中康裕, 矢島麗嘉:日本農芸化学会誌,74,961-966 (2000).
- 特開2011-172582 三井化学株式会社 D-セリン合成活性を有する酵素を利用したD-セリンの製造方法
- 浅野泰久,米田英伸,岡崎誠司,山根隆:生化学,80,294-299 (2008).